ボラティリティ 特定の温度で容易に蒸発する物質の傾向を指します。
その理由は次のとおりです。
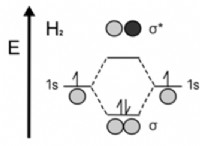
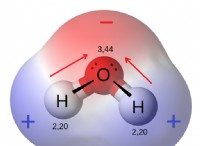
* 分子間力: 分子間の分子間力の強度は、液体がガスに簡単に移行できるかどうかを決定します。分子間力が弱い(ロンドン分散力など)液体はより簡単に蒸発し、揮発性と見なされます。 強い分子間力(水素結合など)を持つ液体は、蒸気圧が低く、揮発性が低くなります。
* 温度: ボラティリティは温度に直接関係しています。温度が上昇するにつれて、分子間力を克服し、気相に逃げるのに十分なエネルギーがあります。
例:
* 揮発性液体: エーテル、ガソリン、アセトン、アルコール。これらは分子間力が弱く、室温ですぐに蒸発します。
* 不揮発性液体: 水(室温)、植物油、蜂蜜。これらは強い分子間の力を持ち、容易に蒸発しません。
重要な注意: 不揮発性の液体でさえ蒸発する可能性がありますが、揮発性液体と比較してはるかに遅い速度でそうします。