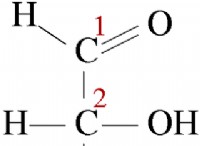
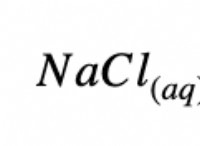* 金属酸化物とその構造: 金属酸化物には通常、金属陽イオン(正の帯電イオン)と酸化物陰イオン(O 2- )。
* 酸との反応: 金属酸化物が酸と反応すると、酸化物陰イオンは水素イオンと反応します(H + )酸から水を形成する(h 2 o)。その後、金属陽イオンは酸から残りのアニオンと結合して塩を形成します。
* 例:
*酸化ナトリウム(Na 2 o)塩酸ナトリウム(NaCl)と水(H 2 と反応して、塩酸(HCl)と反応します。 o):
* Na 2 O + 2 HCl→2 NaCl + H 2 o
* 基本的な性質: 酸と水を形成する酸との反応は、塩基の重要な特徴です。したがって、金属酸化物は基本と見なされます。
ただし、金属酸化物の塩基性が異なる可能性があることに注意することが重要です:
* グループ1および2金属: グループ1および2の金属(アルカリおよびアルカリのアースメタル)の酸化物は、一般に強く基本的です。
* 遷移金属: 遷移金属の酸化物は、さまざまな程度の塩基性を持つ可能性があり、一部の酸性または両性特性を示すものもあります。
* 非金属: 非金属の酸化物は一般に酸性です。
結論: 金属酸化物が酸と反応して塩と水を形成する能力と水は、それらを塩基性として分類します。これは一般的な特性ですが、塩基性は関与する金属によって異なる場合があります。