基本
* 外側の電子: これらは、原子の最も外側のエネルギーレベルの電子であり、価電子とも呼ばれます。彼らは化学結合に関与しているものです。
* 化学結合エネルギー: これは、特定の化学結合を破り、結合した原子を分離するために必要なエネルギーの量です。 結合エネルギーが高いほど、結合が強くなります。
関係
1。魅力と反発: 化学結合の形成には、他の原子の負に帯電した外側電子に対する1つの原子の正に帯電した核の引力と、2つの原子の電子間の反発との間の微妙なバランスが含まれます。
2。安定性: 原子は、電子のより安定した配置を作成する結合を形成する傾向があります。 これには、多くの場合、電子の完全な外殻(貴族のような)を達成することが含まれます。
3。債券の種類:
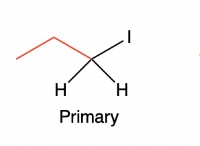
* 共有結合: 原子は外側の電子を共有して、完全な外側のシェルを実現します。結合の強度は、共有電子の数(単一、二重、三重結合)の数に依存します。
* イオン結合: 原子は電子を伝達して正に負に帯電したイオンを形成し、それが互いに引き付けられます。
4。結合強度に影響する要因:
* 電気陰性度: 原子が結合中に電子を引き付ける能力。 電気陰性度の違いが大きいほど、結合は極性と強くなります。
* 原子のサイズ: より小さな原子は一般に強い結合を形成します。
* 債券注文: 原子間の共有電子ペアの数(単一、二重、トリプル)。 債券の順序が高いほど、債券が強くなります。
要約
化学結合エネルギーは、隣接する原子の外側電子間の相互作用の直接的な結果です。 これらの電子の共有または伝達の方法は、形成される結合の強度とタイプを決定します。 外部電子の挙動を理解することは、化学的結合と分子の特性を理解するために重要です。