基本を理解する
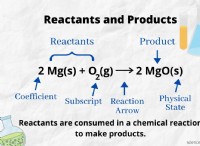
* 化学量論: 化学反応における反応物と産物の間の定量的関係の研究。バランスのとれた化学式に依存して、物質間のモル比を提供します。
* 濃度: 特定の量の溶液に溶解した物質の量。一般的な単位には、モル濃度(1リットルあたりのモル、m)が含まれます。
化学量論を使用して濃度を決定する手順
1。バランスの取れた化学式を書きます: これにより、反応物と生成物の間の正しいモル比が保証されます。
2。既知の未知の量と未知の量を識別します:
* 既知: 通常、1つの反応物または生成物の量(質量、体積、またはモル)に関する情報があります。
* 不明: 溶液中の特定の物質(通常は反応物または生成物)の濃度。
3。化学量論を使用して、既知と未知の量を関連付ける:
*既知の量をモルに変換します(まだモルにない場合)。
*バランスの取れた方程式のモル比を使用して、未知の物質のモルを計算します。
4。濃度を計算します:
*未知の物質のモルを溶液の体積(リットル)で分割します。
例
問題: 250 mLの溶液を作るのに十分な水に2.5 gの水酸化ナトリウム(NaOH)を溶解します。 NaOH溶液のモル濃度はどのくらいですか?
解決策
1。バランスの取れた方程式: 私たちは単一の溶質を扱っているので、この問題には必要ありません。
2。既知および不明:
*既知:2.5 g naoh、250 ml溶液
*不明:NaOHのモル濃度(m)
3。化学量論:
* naOHの質量をモルに変換する:
* NaOHのモル質量=40 g/mol
* naohのモル=(2.5 g) /(40 g / mol)=0.0625 mol
* ボリュームをリットルに変換:
* 250 ml =0.25 l
4。濃度の計算:
*モラリティ(M)=(NaOHのモル) /(リットルの溶液の体積)
*臼歯(m)=(0.0625 mol) /(0.25 l)=0.25 m
したがって、NaOH溶液のモル濃度は0.25 mです。
重要なメモ:
* 単位が重要です: すべての測定が一貫したユニット(グラム、ほくろ、リットルなど)にあることを確認してください。
* 制限反応物: 複数の反応物との反応では、形成できる生成物の最大量を決定するため、制限反応物を特定します。
* 滴定: これは、既知の濃度の溶液と反応することにより、溶液の濃度を決定するために使用される一般的な手法です。化学量論は滴定計算に不可欠です。