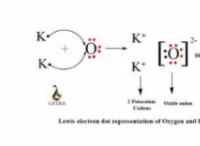
違いを理解する
* イオン固体:
*正の帯電イオン(陽イオン)と負に帯電したイオン(アニオン)の間の静電魅力によって形成されます。
*通常、強い静電相互作用により、高い融点と沸点があります。
*溶媒分子はイオンと相互作用して分離できるため、極性溶媒(水のような)に溶けます。
*溶融または溶解したときに電気を伝達します(イオンが自由に移動できるため)。
* 分子固体:
*中性分子間の弱い分子間力(ファンデルワールス力、水素結合、または双極子双極子相互作用など)によって形成されます。
*通常、イオン固体と比較して、融点と沸点が低くなります。
*分子間力が類似しているため、しばしば非極性溶媒(ヘキサンなど)に溶けます。
*どの州でも電力を導かないでください。
実験技術
1。融点と沸点:
* 手順: 未知の固体の小さなサンプルを慎重に加熱し、その融点と沸点を観察します。
* 解釈: イオン固体は通常、融点と沸点が高い(多くの場合300°Cを超える)。分子固体は、融点と沸点が低い。
2。溶解度:
* 手順: 水中の固体の溶解度とヘキサンのような非極性溶媒をテストします。
* 解釈:
*イオン固体はしばしば水(極性溶媒)に溶けますが、通常は非極性溶媒には不溶です。
*分子固体はしばしば非極性溶媒に溶けますが、水には溶解性が低くなる可能性があります。
3。電気伝導率:
* 手順: 固体の固体、溶融状態の導電率をテストし、水に溶解します(可溶性の場合)。
* 解釈:
*イオン固体は、溶融または水に溶解したときに電気を伝達しますが、固体状態ではありません。
*分子固体はどの状態でも電気を導入しません。
4。分光分析:
* 手順: X線回折などの技術を使用して、固体内の原子の配置を決定できます。
* 解釈: イオン固体のX線回折パターンは、しばしば高度に秩序化された繰り返し構造を示しますが、分子固体は秩序化されたパターンを示す可能性があります。
追加の考慮事項:
* 外観: イオン固体はしばしば結晶性です(通常の幾何学的な形状を持っています)。分子固体は、結晶またはアモルファスになる可能性があります(通常の形状がありません)。
* 化学組成: 固体に存在する要素を知ることは、その結合についての手がかりを提供することがあります。たとえば、固体に金属と非金属が含まれている場合、イオン性である可能性があります。
重要な注意: これらの技術はイオン固体と分子固体を区別するのに役立ちますが、それらは絶対確実ではありません。一般的なルールには例外があり、一部の化合物はイオン結合と分子結合の両方の特性を示す場合があります。