1。化学的違い:
* イオン組成: 2つのソリューションには異なるイオン組成があります。
* KCL+NABR:K+、Cl-、Na+、およびBr-イオンが含まれています。
* KBR+NACL:K+、Br-、Na+、およびCl-イオンが含まれています。
* 化学反応: 両方の溶液には同じイオンが含まれていますが、存在するイオンの特定の組み合わせは、潜在的な化学反応につながる可能性があります。たとえば、特定の触媒が存在する場合、溶液は二重変位反応を受ける可能性があり、それぞれKClとNABRまたはKBRとNaClの形成につながります。
2。身体的な違い:
* 結晶化: 2つのソリューションは異なって結晶化します。 KCl + NABRは潜在的にKClとNABR結晶の混合物を形成し、KBR + NaClはKBR結晶とNaCl結晶の混合物を形成します。
* 溶解度: 水中のKCL、NABR、KBR、およびNaClの個々の溶解度は、全体的なモル密度が同じにもかかわらず、わずかに異なる場合があります。 これは、個々のイオンの濃度が2つの溶液で異なる可能性があることを意味します。
* 密度: 2つの溶液の密度は、溶液中のイオンが異なるため、わずかに異なる場合があります。この違いは小さくなりますが測定可能です。
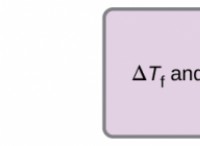
* 衝突特性: 凍結点のうつ病や沸点の上昇などの衝突特性は、溶解した粒子の総数に依存します。 総モル密度は同じですが、単位体積あたりの粒子の数は、イオン相互作用と水和効果の変動により、わずかに異なる場合があります。
要約:
2つの溶液の全体的なモル密度は同じかもしれませんが、イオンの特定の組み合わせとその相互作用により、異なる化学的および物理的特性が生じます。
重要な注意: これらの違いは一般に微妙です。より具体的な詳細に興味がある場合、または特定の条件下で2つのソリューションを比較する場合は、各塩の実際の濃度と興味のある特定の特性を考慮する必要があります。