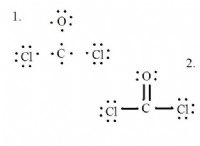その理由は次のとおりです。
* 電気陰性度: フッ素は、周期表で最も電気陰性の要素です。電気陰性度とは、原子が電子を引き付ける傾向です。電気陰性度が高いほど、原子は電子をより強く引き付けます。
* 結合強度: F2のF-F結合は、CL2のCl-CL結合よりも弱いです。これにより、F2がバラバラになり、新しい結合を形成しやすくなり、反応性が高くなります。
* 原子サイズ: フッ素は塩素よりも小さい。このサイズが小さくなると、フッ素が他の原子に近づき、結合を形成しやすくなります。
要約すると、高い電気陰性度、結合強度が低く、原子サイズが小さくなると、フッ素(F2)が塩素(CL2)よりも化学的に活性になります。