1。電子を獲得する傾向:
*非金属は一般に高い電気陰性度を持っています。つまり、電子に強い魅力があります。
*安定した電子構成を実現するために(Nobleガスのように)、それらは電子を *獲得 *する傾向があり、アニオンと呼ばれる陰イオンを形成 。
2。共有結合の形成:
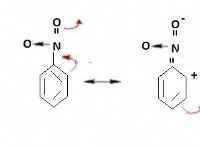
*非金属は他の非金属と電子を共有して共有結合を形成します 。この共有により、両方の原子が安定した電子構成を実現できます。
*共有結合は、共有された電子の数に応じて、単一、二重、または三重の結合にすることができます。
3。分子化合物の形成:
*非金属結合が共有結合すると、分子化合物を形成します 、それは弱い分子間力によって一緒に保持されます。
*これらの分子は、多くの場合、室温でのガスまたは液体であり、熱と電気の導体が貧弱である傾向があります。
4。反応性の多様性:
*非金属は一般に電子を獲得する傾向がありますが、反応性は大幅に異なります。
*一部の非金属は非常に反応性があり(フッ素や酸素など)、比較的不活性(窒素や貴族など)があります。
5。具体的な例:
* ハロゲン: 負のイオン(ハロゲン化物)を容易に形成する高反応性の非金属。
* 酸素: 燃焼や多くの生物学的プロセスに不可欠です。
* 窒素: 大気の主要な要素と人生に不可欠です。
注: これらは一般的な傾向であり、例外があります。一部の非金属は、金属とのイオン結合を形成することもあり、一部は金属特性を示すことさえできます。
要約すると、非金属は、電子を獲得し、共有結合を形成し、分子化合物を生成する傾向によって特徴付けられます。それらの反応性は大きく異なりますが、多くの化学プロセスで重要な役割を果たしています。