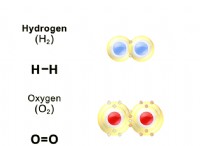
この原理が化学式のバランスをとるのに役立つ方法は次のとおりです。
1。要素を識別します: 反応物と生成物に存在するすべての要素をリストすることから始めます。
2。カウント原子: 方程式の両側に各要素の原子の数をカウントします。
3。係数を調整します: 各要素の原子の数が両側で同じであることを確認するには、各化学式の前の係数を調整する必要があります。係数は、反応に関与する各物質の分子の数を表します。
例:
メタンの燃焼の不均衡な方程式を見てみましょう。
ch₄ +o₂→co₂ +h₂o
* ステップ1: 元素は、炭素(C)、水素(H)、および酸素(O)です。
* ステップ2:
*反応物:1 c、4時間、2 o
*製品:1 c、2時間、3 o
* ステップ3: バランスを取るには、係数を調整します。
* 1Ch₄ +2o₂→1CO₂ +2H₂O
これで、各要素の原子の数は両側で等しくなります。
* 反応物: 1 c、4時間、4 o
* 製品: 1 c、4時間、4 o
化学式のバランスが不可欠です:
*それは、質量の保全法則が支持されることを保証します。
*それは正確な化学量論比を与えます。これは重要です。
*反応に関与する反応物と生成物の量を予測する。
*化学反応における理論的収量の計算。
*化学反応における物質間の定量的関係を理解する。
化学的方程式のバランスをとる例をもっと見たい場合は、お知らせください!