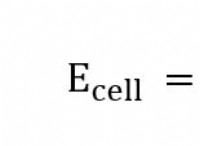* バイナリ化合物とは? バイナリ化合物は、2つの要素から形成された化合物です。
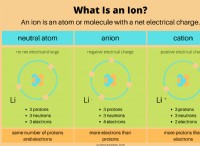
* イオンとは? イオンは、電子を獲得または失った原子または分子であり、正味の電荷を引き起こします。
これがプロセスです:
1。溶解: バイナリ化合物が水に溶けると、その分子またはイオン単位がバラバラになり、水分子に囲まれます。
2。解離: 化合物がイオンの場合 、正に帯電した陽イオンと負に帯電した陰イオンの間の静電力は、極水分子によって弱くなります。これにより、化合物は個々のイオンに解離します。たとえば、塩化ナトリウム(NaCl)を水に溶解してNa+およびCl-イオンを形成します。
3。伝導: 溶液中のこれらの遊離イオンは、電界の影響下で移動できます。陽イオンは負の電極(カソード)に向かって移動し、陰性イオンは正の電極(アノード)に向かって移動します。この荷電粒子の流れは電流を構成し、溶液が電気を導入できるようにします。
キーポイント:
* すべてのバイナリ化合物が溶液中に電気を伝導するわけではありません。 イオンに分離するもののみ 実施します。
* 共有結合バイナリ化合物 一般に、水中のイオンに分離しないため、電気の導体が貧弱です。例には、水(H₂O)と二酸化炭素(CO₂)が含まれます。
* イオンバイナリ化合物 通常、水中のイオンに分離し、電気の良好な導体です。例には、塩化ナトリウム(NaCl)、臭化カリウム(KBR)、および酸化マグネシウム(MGO)が含まれます。
要約すると、電気を伝導するバイナリ化合物の水溶液の能力は、水に溶解したときにイオンを形成する能力に依存します。イオンに解離する化合物のみが、電流の流れを促進できます。