* 極性: 水分子は極性です。つまり、わずかに正の末端(水素原子)とわずかに負の末端(酸素原子)があります。これにより、分子内に部分的な電荷分離が作成されます。
* 水素結合: 水分子のわずかに陽性の水素原子は、他の水分子のわずかに負の酸素原子に引き付けられ、強い水素結合を形成します。これらの結合は、液体状態に水分子を一緒に保持します。
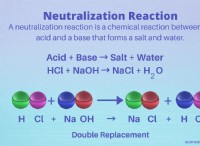
* 溶質との相互作用: 塩(NaCl)または砂糖(スクロース)が水に加えられると、極水分子は溶質のイオンまたは分子を囲みます。
* 塩: 水分子は、正に帯電したナトリウムイオン(Na+)と負に帯電した塩化物イオン(Cl-)の塩を囲み、結晶構造にそれらをまとめるイオン結合を効果的に壊します。
* 砂糖: 水分子は、糖分子のヒドロキシル基(-OH)と水素結合を形成します。この相互作用は、糖分子間の結合を弱め、溶解することができます。
本質的に、水の極性と水素結合を形成する能力により、イオン化合物(塩など)と極性分子(砂糖など)の両方と良好に相互作用し、効果的に引き離して溶解することができます。