その理由は次のとおりです。
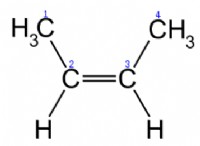
* ヘキサン(C6H14) 非極性分子です。炭素と水素の原子のみを備えた対称構造を持っています。これらの結合は非極性であり、分子自体には全体的な双極子モーメントがありません。
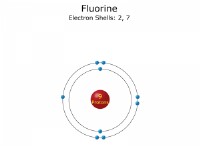
* ジクロロメタン(CH2CL2) 極分子です。炭素と塩素の間の電気陰性度の違いにより、炭素塩素結合は極性です。これにより、分子に正味の双極子モーメントが作成されます。
極性 分子内の電子密度の不均一な分布の尺度です。より多くの電気陰性の原子が電子を自分自身に向けて引っ張り、部分的な負電荷を作成します。逆に、電気陰性の原子が少ないほど、部分的な正電荷があります。この充電の違いは、双極子モーメントを作成します。
ジクロロメタンは極性C-C-C-CL結合のために有意な双極子モーメントを持っているため、ヘキサンよりも極性と見なされます。