1。トリプルボンド強度: N2分子の窒素原子は、最も強力な化学結合の1つである強力な三重結合によってまとめられています。 N2のN-N結合の結合解離エネルギーは約946 kJ/molであり、F2(159 kJ/mol)のF-F結合の結合解離エネルギーと比較してはるかに高いです。この強力なトリプル結合により、窒素は多くの化学反応に対する反応性を低下させます。
2。フッ素の高い電気陰性度: フッ素は周期表で最も電気陰性の要素であり、電子を引き付ける傾向が強いことを意味します。この高い電気陰性度により、フッ素は窒素を含む他の元素と容易に結合することができます。対照的に、窒素は電気陰性度が低いため、他の元素との結合形成に関与する可能性が低くなります。
3。不活性ペア効果: 窒素の場合、最も外側の電子(2p電子)はペアになり、比較的安定しています。この現象は、不活性ペア効果として知られています。この効果により、窒素の最も外側の電子は他の原子との結合に使用できなくなり、反応性が低下します。一方、フッ素は有意な不活性なペア効果を示さず、その最も外側の電子は結合形成にアクセスしやすいです。
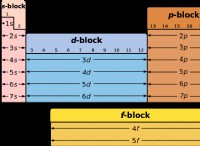
4。 d軌道の欠如: 窒素原子には、原子価殻にD軌道がありません。これにより、特定の種類の化学反応に参加する能力が制限されています。 d軌道は、配位錯体やPIバックボンディングなど、多くの重要な結合相互作用に不可欠です。一方、フッ素はグループ17に属し、D軌道を含む完全な原子価軌道を持っているため、より幅広い化学反応に従事することができます。
5。分子サイズ: 窒素分子(N2)は、フッ素分子(F2)と比較して比較的小さく、コンパクトです。 N2のコンパクトな構造により、他の分子や原子が反応することができなくなり、全体的な反応性が低下します。サイズが小さく、フッ素分子は表面積が大きく、他の物質との相互作用にアクセスしやすく、反応性が高くなります。
要約すると、強い三重結合、フッ素の高い電気陰性度、不活性なペア効果、D軌道の欠如、および分子サイズの違いの組み合わせは、フッ素と比較して気体窒素の反応性の低下に寄与します。