これが故障です:
* イオン結合: 硫黄は、ナトリウム(NA)やカリウム(K)などの金属とイオン結合を形成できます。これらの場合、硫黄は電子を摂取して硫化物イオン(S²⁻)を形成します。これは、硫黄が金属よりも電気陰性であるため、電子をより強く引っ張っているためです。
* 共有結合: 硫黄は、酸素(O)や塩素(CL)など、他の非金属と共有結合を形成することもできます。これらの場合、硫黄は他の非金属と電子を共有します。これは、硫黄や他の非金属が類似した電気陰性度値を持っているため、電子がかなり均等に共有されているためです。
例:
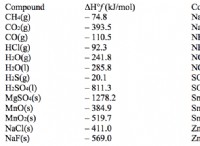
* 硫化ナトリウム(Na₂s): ナトリウム金属と硫黄の反応によって形成されるイオン化合物。
* 二酸化硫黄(SO₂): 硫黄と酸素の反応によって形成される共有化合物。
したがって、結合硫黄形式のタイプは、それが反応している要素に依存します。