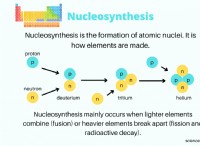
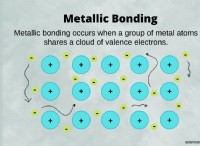
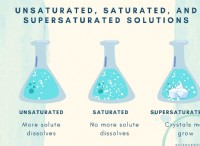
1。ステアリン酸ナトリウムとは?
ステアリン酸ナトリウムは、長鎖脂肪酸であるステアリン酸のナトリウム塩です。石鹸や洗剤の一般的な成分です。
2。ステアレート陰イオンの加水分解:
ステアル酸ナトリウムが水に溶けると、ステアレートアニオン(C17H35COO-)は加水分解を受けます。これは、水分子と反応し、プロトン(H+)を引っ張ることを意味します。
c17h35coo- + h2o⇌C17H35COOH + OH-
この反応で:
*ステアレートアニオン(C17H35COO-)は、水からプロトンを受け入れ、ステアリン酸(C17H35COOH)を形成します。
*これにより、溶液中に水酸化物イオン(OH-)が残ります。
3。結果:アルカリ溶液
溶液中の水酸化物イオン(OH-)の存在は、アルカリ性になります。ステアリン酸ナトリウム溶液のpHは7を超えており、そのアルカリ性を示しています。
4。なぜ加水分解が起こるのか?
ステアリン酸アニオンは、弱酸(ステアリン酸)の共役底部です。 弱酸は陽子を供与する傾向があります。つまり、その共役塩基は陽子を容易に受け入れます。これにより、加水分解反応が促進されます。
要約すると、ステアリン酸ナトリウム溶液は、溶液中に水酸化物イオン(OH-)を生成するステアリン酸アニオンの加水分解のためにアルカリ性です。