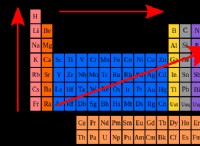
1。電気陰性度: 酸素は非常に電気陰性であり、電子に強い魅力を持っていることを意味します。これにより、多くの場合、他の原子を犠牲にして電子を獲得することが非常に熱心になります。
2。二重結合: 酸素は、その二等層(O2)でそれ自体と二重結合を形成し、分子を比較的不安定にします。この不安定性は、酸素を促進し、より安定した構成を実現するために電子を探します。
3。小さいサイズ: 酸素の小さなサイズにより、その核は電子を強く引き付けることができ、電気陰性度をさらに高めます。
4。空の軌道の豊富さ: 酸素には、外側のシェルに2つの対応のない電子があり、電子を獲得して結合を形成するために高い親和性を与えます。
酸化の仕組み:
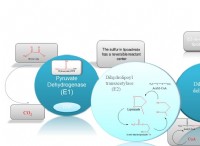
酸素が酸化剤として作用すると、別の物質から電子を受け入れます。このプロセスにより、他の物質から電子が失われ、「酸化」されると言われます。
酸素の酸化力の例:
* 錆び: 鉄は、水の存在下で酸素と反応して酸化鉄(錆)を形成します。これは、鉄が酸化されるプロセスです。
* 燃焼: 燃料燃料は酸素との迅速な反応を伴い、熱と光の形でエネルギーを放出します。
* 呼吸: 生物は酸素を利用してグルコースを酸化し、ATPの形でエネルギーを生成します。
重要な注意: 酸素は強い酸化剤ですが、酸素を含むすべての反応が燃焼ではないことを覚えておくことが重要です。酸素は幅広い反応に関与しており、その一部は生命に不可欠です。