その理由は次のとおりです。
* 発熱反応 通常は熱として、周囲にエネルギーを放出します。これは、製品のエネルギーが反応物よりも低いことを意味し、エンタルピー(ΔH)の全体的な変化を負にすることを意味します。
* 強い結合 製品では、それらを壊すにはより多くのエネルギーが必要であることを示しています。つまり、より安定しています。 これらの強力な結合を形成するときに放出されるエネルギーは、反応物の弱い結合を破壊するために吸収されたエネルギーよりも大きくなります。
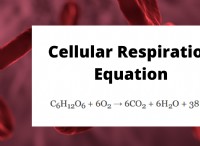
例: メタン(CH4)のような燃料の燃焼は発熱反応です。製品の結合(CO2およびH2O)の結合は、反応物の結合よりも強く、熱と光の放出につながります。
キーポイント:
* 発熱反応: エネルギーを放出、ΔH<0
* 吸熱反応: エネルギーを吸収、ΔH> 0
* より強い結合: より高い結合エネルギー、より安定しています
化学反応についてこれ以上質問がある場合はお知らせください!